Génie chimique
Concevez, élaborez et analysez les machines de traitement, y compris les réacteurs, les chaudières et les pompes. Résolvez les problèmes de transfert de chaleur et concevez des systèmes de commande.
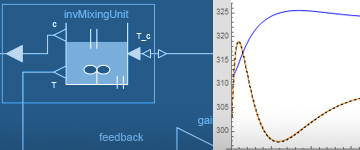
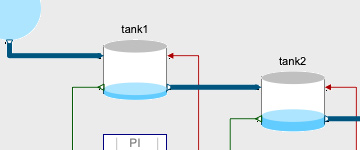
Unité de mélange contrôlée
Un problème de commande important consiste à concevoir des contrôleurs pour des systèmes non linéaires à l’aide d’une commande d’inversion de modèle. L’exemple suivant utilise une composante InverseBlockConstraints pour construire facilement des modèles inverses. Il utilise également la bibliothèque Modelica_Synchronous pour discrétiser automatiquement le contrôleur feedforward non linéaire à temps continu.

Réactions chimiques
Lors d’une expérience chimique, il est utile de savoir quelle quantité de produit vous obtiendrez lorsque vous mélangez certaines quantités de réactifs. Ceci est particulièrement utile dans le monde réel, par exemple dans la production ou l’analyse chimique. Dans cet exemple, vous apprendrez à prédire le résultat d’une réaction, compte tenu des quantités initiales de réactifs et du rapport entre les produits et les substrats.
Équilibre chimique
La plupart des réactions chimiques ne sont pas irréversibles et se déroulent en fait dans les deux sens. Cependant, toutes les réactions réversibles atteignent un état d’équilibre dans lequel les concentrations des substrats au sein de la réaction deviennent constantes. Dans cet exemple, vous apprendrez à modéliser une réaction chimique réversible et à analyser la dynamique de la réaction. Vous apprendrez à connaître les constantes d’équilibre et les vitesses de réaction.
Équilibre hétérogène
L’équilibre hétérogène fait référence aux réactions réversibles dans lesquelles les substrats des réactions se trouvent dans des phases différentes. L’un des types de réactions les plus utiles est celui où un solide est dissous dans une solution aqueuse. Dans cet exemple, vous apprendrez ce qu’est l’équilibre hétérogène et comprendrez le concept de solubilité.
Lois de vitesse
Les réactions chimiques se produisent à des rythmes différents et leur vitesse varie considérablement. Certaines réactions se produisent très rapidement, par exemple une explosion ou la combustion de carburant dans une voiture de course. Dans cet exemple, vous allez travailler sur la cinétique chimique et l’étude des vitesses des processus chimiques. Vous apprendrez à calculer la vitesse, l’ordre de réaction et la demi-vie d’une réaction.
Wolfram System Modeler
Essayez
Achetez
System Modeler est disponible en anglais
et en japonais
sur Windows, macOS et Linux »
Vous avez des questions ou des commentaires ? Contactez un expert Wolfram »